هیچ محصولی در سبد خرید نیست.
سلول گالوانی نوعی از سلولهای الکتروشیمیایی به شمار میآید که به منظور تامین جریان الکتریکی از آن استفاده میشود. این تامین جریان از طریق انتقال الکترونها به کمک واکنشهای اکسایش و کاهش صورت میگیرد.
به ظرفی که در آن واکنش اکسایش و کاهش به شکل کنترل شده انجام میشود، سلول گفته میشود. هرسلول از دو نیمسلول تشکیل شده است.
- نیمسلول آند محل انجام اکسایش است.
- نیمسلول کاتد محل انجام کاهش است.
برای آشنایی بیشتر با سلول گالوانی و الکترولیتی توصیه میکنم کلیپ زیر، که بخشی از فیلم حل تست شیمی دوازدهم است را تماشا کنید:
اجزای سلول گالوانی
- دو الکترود رسانا دارد که به وسیله سیمی رسانا بهم دیگر وصل میشود.
- دو محلول یونی
- یک دیواره متخلخل که بین دو محلول یونی قرار گرفته است.
تعیین آند و کاتد در سلول گالوانی
- نیمسلولی که پتانسیل کاهش (E۰) بیشتری دارد، کاتد است و در آن نیمواکنش کاهش انجام میشود.
- نیمسلولی که E۰ کمتری دارد، آند است و در آن نیمواکنش اکسایش انجام میشود.
- نکته: در سلول گالوانی، کاتد قطب مثبت و آند قطب منفی محسوب میشوند.
نکته: در سلول گالوانی در اثر انجام واکنش اکسایش-کاهش انرژی تولید میشود که به صورت انرژی الکتریکی جمعآوری میشود.
نمایی از سلول گالوانی Zn-Cu
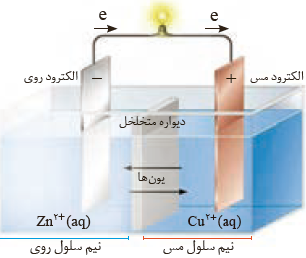
در این سلول گالوانی : E۰(Cu+/Cu) > E۰(Zn۲+/Zn)
پس نیم سلول مس کاتد و نیم سلول روی آند است.
در آند نیم واکنش اکسایش انجام میشود:
![]()
در کاتد نیمواکنش کاهش انجام میشود:
![]()
واکنش کلی به شکل زیر میشود:
![]()
تغییرات جرم الکترودها و غلظت یونها در سلول گالوانی
- در آند جرم الکترود کاهش یافته و غلظت یون مثبت افزایش مییابد. (در اثر اکسایش)
- در کاتد جرم الکترود افزایش یافته و غلظت یون مثبت کاهش مییابد. (در اثر کاهش)
جهت حرکت الکترونها در سیم
- در آند الکترونها از الکترود به سیم منتقل میشوند.
- این الکترونها در سیم مسیرشان را از آند به سمت کاتد طی میکنند.
- در کاتد الکترونها از سیم به الکترود وارد میشوند.
یک غشا به نام دیواره متخلخل بین آند و کاتد است که یونها را به صورت انتخابی از خود عبور میدهد.
وظایف دیواره متخلخل
- مانع مخلوط شدن ناگهانی محلول ها میشود.
- محلولها را از نظر بار الکتریکی خنثی نگهمیدارد.
در کاتد سلول غلظت یون مثبت +Cu کم میشود (جذب الکترود میشود) و بار کلی محلول در این نیم سلول منفی میشود. در این حالت دیواره متخلخل یون نظارهگر متصل به +Cu (مثلا –NO۳) را از خود عبور میدهد تا محلول خنثی بماند.
در آند هم غلظت یون مثبت +Zn۲ در حال افزایش است و بار کلی محلول در این نیمسلول مثبت میشود. در این حالت دیواره متخلخل یون مثبت +Zn۲ را از خود عبور میدهد تا محلول خنثی بماند.
نکته: در سلول گالوانی از دیواره متخلخل آنیون به سمت آند و کاتیون به سمت کاتد میرود.

فلش کارت بالا، نمونهای از فلشکارتهای جامع شیمی ماست و باعث میشود شیمی کنکور را دیگر فراموش نکنید! برای اطلاعات بیشتر روی فلشکارت شیمی کلیک کنید.
نیروی الکتروموتوری (emf)
- به اختلاف پتانسیلی که باعث ایجاد جریان میشود، نیروی الکتروموتوری گفته میشود.
- این نیرو با ولت (V) گزارش میشود.
- به این نیرو، E۰ سلول هم گفته میشود.
- این نیرو به شکل زیر محاسبه میشود.
![]()
که در سلول گالوانی قطب مثبت کاتد و قطب منفی آند است، پس محاسبه emf به شکل زیر میشود:
![]()
و چون در سلول گالوانی E۰ کاتد بزرگتر از E۰ آند است، emf در آنها همیشه عددی مثبت است.
در صورتی که برای شیمی سال دوازدهم، نیاز به یک آموزش جامع و مفهومی دارید، استفاده از بسته مفهومی شیمی دوازدهم را به شما توصیه میکنم. برای اطلاعات بیشتر بر روی تصویر زیر کلیک کنید:

دانلود فایل PDF خلاصهای از سلول گالوانی شیمی دوازدهم
در انتهای توصیه میکنم به مطالب زیر هم سر بزنید:
- خلاصه ای از سلول الکترولیتی
- خلاصه ای از آنتالپی
برای دریافت مطالب کنکوری بیشتر، عضو کانال تلگرام شیمی کنکور و پیج اینستاگرام شیمی ما بشوید و برای تماشای کلیپ های آموزشی به کانال آپارات ما نیز مراجعه کنید.
اگر شما هم راجع به ” سلول گالوانی شیمی دوازدهم ” سوالی دارید، زیر همین پست بنویسید. قول می دهیم تا جای ممکن پاسخ دهیم.











