سبد خرید شما خالی است.
برخی از سلولها هستند که با انجام واکنشهای اکسایش – کاهش در آنها انرژی تولید میشود (مثل سلول گالوانی). نوع دیگری از سلولهای الکتروشیمیایی وجود دارند که با اعمال یک ولتاژ بیرونی و عبور جریان الکتریکی از درون محلول الکترولیت، میتوان یک واکنش شیمیایی را در خلاف جهت طبیعی پیش راند (از انرژی الکتریکی به انرژی شیمیایی میرسیم). به این سلولها، سلولهای الکترولیتی میگویند. برقکافت آب یک نمونه از واکنشهایی است که در سلول الکترولیتی انجام میشود.
کاربردهای سلول الکترولیتی
- برقکافت: یعنی جدا کردن عنصرهای سازنده یک ماده از همدیگر.
- آبکاری: یعنی ایجاد یک روکش فلزی بر روی سطح یک جسم رسانا.
مقایسه سلول الکترولیتی و گالوانی

اجزای سلول الکترولیتی
- یک محلول یا مذاب یونی (یک نوع)
- باتری
- دو الکترود (تیغه): الکترود شماره ۱، قطب منفی است و به الکترود کوتاه باتری متصل میشود. الکترود شماره ۲، قطب مثبت است و به الکترود بلند باتری متصل میشود.

نحوه کارکرد سلول الکترولیتی
- با برقراری جریان توسط باتری بین الکترودها میدان الکتریکی تشکیل میشود.
- درون الکترولیت یونهای مثبت و منفی جهتگیری کرده و به سوی قطبهای ناهمنام حرکت میکنند.
- در قطب مثبت سلول، یونهای منفی با از دست دادن الکترون، اکسید میشوند. پس قطب مثبت آند سلول الکترولیتی است.
- در قطب منفی سلول، یونهای مثبت الکترون دریافت میکنند و کاهش پیدا میکنند. پس قطب منفی کاتد سلول الکترولیتی است.
برقکافت آب، راهی برای تولید گاز هیدروژن
- الکترولیت این سلول آب است.
- در بالای الکترودهای الکترود لوله آزمایش قرار میگیرد، علت آن این است که فراوردههای این واکنش گازی هستند.
- حجم هریک از این گازها که در بالای این الکترودها جمع میشود متفاوت است.

عملکرد برقکافت آب
۱- در آند این سلول که به قطب مثبت باتری متصل است، مولکولهای آب الکترون از دست داده و گاز اکسیژن تولید میکنند.
نیمواکنش اکسایش:
![]()
۲- در کاتد این سلول، مولکولهای آب الکترون میگیرند و گاز هیدروژن تولید میشود.
نیمواکنش کاهش:
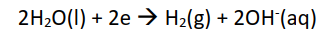
واکنش کلی:
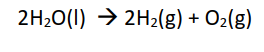
حجم گازهای تولید شده حاصل از برقکافت
با توجه به واکنش کلی، حجم گاز هیدروژن تولید شده دو برابر حجم گاز اکسیژن تولید شده است.
بررسی pH در اطراف الکترودها
- باتوجه به نیمواکنش کاهش در اطراف کاتد– OH تولید میشود و در این ناحیه محلول خاصیت بازی دارد.
- در نیمواکنش اکسایش در اطراف آند هم+H تولید میشود و در این ناحیه محلول خاصیت اسیدی دارد.
بهبود عملکرد سلول
- حتی خالصترین آبها هم به دلیل خودیونش آب دارای مقادیر کمی از یونهای هیدرونیم (+H) و هیدروکسید (–OH) هستند.
- درنتیجه آب خالص هم دارای خاصیت رسانایی میباشد.
- اما به علت کم بودن غلظت این یونها، آب خالص رسانایی ضعیفی دارد.
- پس برای افزایش رسانایی و بهبود عملکرد این سلول، باید مقدار اندکی الکترولیت به آب افزود.
در صورتی که برای شیمی سال دوازدهم، نیاز به یک آموزش جامع و مفهومی دارید، استفاده از بسته مفهومی شیمی دوازدهم را به شما توصیه میکنم. برای اطلاعات بیشتر بر روی تصویر زیر کلیک کنید:

دانلود فایل PDF خلاصهای از سلول الکترولیتی شیمی دوازدهم
برای دریافت مطالب کنکوری بیشتر، عضو کانال تلگرام شیمی کنکور و پیج اینستاگرام شیمی ما بشوید و برای تماشای کلیپ های آموزشی به کانال آپارات ما نیز مراجعه کنید.
اگر شما هم راجع به ” سلول الکترولیتی شیمی دوازدهم ” سوالی دارید، زیر همین پست بنویسید. قول می دهیم تا جای ممکن پاسخ دهیم.











